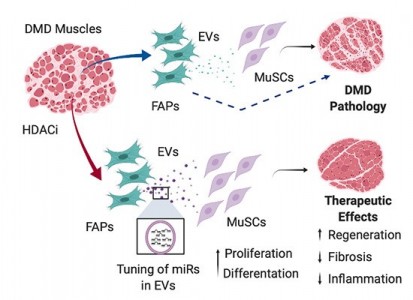
 图: HDAC抑制剂处理后的DMD肌肉中的FAP细胞释放细胞外囊泡,囊泡中的microRNA通过调节DMD发病机制中的各个方面而带来治疗作用。 细胞间的通讯障碍 课题组先前的研究表明,随着DMD的发展,称为纤维脂肪形成祖细胞(FAP)的特殊肌肉愈合细胞被破坏,并开始促进肌肉消减和纤维化。研究团队怀疑,FAP和肌肉干细胞之间的交流改变(可能通过细胞外囊泡)可能是发病原因。 为了回答这个问题,该研究的第一作者MartinaSandonà博士和她的同事们进行了一系列实验,其中包括来自DMD患病男孩的肌肉活检,他们参加了HDACi治疗的临床试验,小鼠DMD模型也用于研究中。科学家能够证明,随着DMD的发展,通过细胞外囊泡进行的细胞通讯随着时间的推移而逐渐改变,从而削弱了DMD肌肉的再生潜力。重要的是,研究人员证明了用HDAC抑制剂纠正细胞外囊泡的含量可以激活肌肉干细胞并促进再生,同时减少纤维化和炎症。该研究的共同通讯作者、圣卢西亚基金会团队负责人、天主教圣心大学终身教授ValentinaSaccone博士说:“我们的发现可能会扩展到其他疾病,将药理化的细胞外囊泡用作再生医学的一般治疗工具。这些颗粒还可以用作其他治疗的辅助方法,例如基因或细胞疗法。”希望与曙光对于患有DMD的人及其家人来说,还需要更快的治疗。这种遗传病是由于肌营养不良蛋白缺乏引起的,肌营养不良蛋白是一种增强肌肉并导致进行性肌肉变性的蛋白质。DMD主要影响男孩,症状通常出现在3到5岁之间。随着医学进步,DMD儿童现在通常可以生存到十几岁到30多岁,但是仍然需要有效的治疗方法。“对于DMD患者及其家人,新研究给他们带来了更美好的希望,”Parent Project Italy的创始人Filippo Buccella说。过去20年来,Puri的研究团队一直为他们提供支持。“这项研究发现了一种有前途的DMD新治疗方法,使我们离治疗方法更近了一步,该方法可以帮助儿童尽可能长时间地保持肌肉力量并维持较好的生活质量。”肌肉萎缩症协会的首席研究官Sharon Hesterlee博士说:“我们治疗DMD的选择越多越多,因为结合不同作用机制的各种药物可能更有效。Puri博士的研究展示了一种独特的方法,可以证明不同药物的互补可以更好地实现疾病治疗。” 参考文献:Sandonà M, Consalvi S, Tucciarone L,et al. (2020) HDAC inhibitors tune miRNAs in extracellular vesicles of dystrophic muscle-resident mesenchymal cells. EMBO Rep 21(9):e50863.
图: HDAC抑制剂处理后的DMD肌肉中的FAP细胞释放细胞外囊泡,囊泡中的microRNA通过调节DMD发病机制中的各个方面而带来治疗作用。 细胞间的通讯障碍 课题组先前的研究表明,随着DMD的发展,称为纤维脂肪形成祖细胞(FAP)的特殊肌肉愈合细胞被破坏,并开始促进肌肉消减和纤维化。研究团队怀疑,FAP和肌肉干细胞之间的交流改变(可能通过细胞外囊泡)可能是发病原因。 为了回答这个问题,该研究的第一作者MartinaSandonà博士和她的同事们进行了一系列实验,其中包括来自DMD患病男孩的肌肉活检,他们参加了HDACi治疗的临床试验,小鼠DMD模型也用于研究中。科学家能够证明,随着DMD的发展,通过细胞外囊泡进行的细胞通讯随着时间的推移而逐渐改变,从而削弱了DMD肌肉的再生潜力。重要的是,研究人员证明了用HDAC抑制剂纠正细胞外囊泡的含量可以激活肌肉干细胞并促进再生,同时减少纤维化和炎症。该研究的共同通讯作者、圣卢西亚基金会团队负责人、天主教圣心大学终身教授ValentinaSaccone博士说:“我们的发现可能会扩展到其他疾病,将药理化的细胞外囊泡用作再生医学的一般治疗工具。这些颗粒还可以用作其他治疗的辅助方法,例如基因或细胞疗法。”希望与曙光对于患有DMD的人及其家人来说,还需要更快的治疗。这种遗传病是由于肌营养不良蛋白缺乏引起的,肌营养不良蛋白是一种增强肌肉并导致进行性肌肉变性的蛋白质。DMD主要影响男孩,症状通常出现在3到5岁之间。随着医学进步,DMD儿童现在通常可以生存到十几岁到30多岁,但是仍然需要有效的治疗方法。“对于DMD患者及其家人,新研究给他们带来了更美好的希望,”Parent Project Italy的创始人Filippo Buccella说。过去20年来,Puri的研究团队一直为他们提供支持。“这项研究发现了一种有前途的DMD新治疗方法,使我们离治疗方法更近了一步,该方法可以帮助儿童尽可能长时间地保持肌肉力量并维持较好的生活质量。”肌肉萎缩症协会的首席研究官Sharon Hesterlee博士说:“我们治疗DMD的选择越多越多,因为结合不同作用机制的各种药物可能更有效。Puri博士的研究展示了一种独特的方法,可以证明不同药物的互补可以更好地实现疾病治疗。” 参考文献:Sandonà M, Consalvi S, Tucciarone L,et al. (2020) HDAC inhibitors tune miRNAs in extracellular vesicles of dystrophic muscle-resident mesenchymal cells. EMBO Rep 21(9):e50863.| 欢迎光临 外泌体之家 | 细胞外膜泡领域核心平台—exosomes & microvesicles—小膜泡大作用 (http://exosome.com.cn/) | Powered by Discuz! X3.3 |