外泌体之家 | 细胞外膜泡领域核心平台—exosomes & microvesicles—小膜泡大作用
标题: Cell Reports: 肿瘤相关巨噬细胞EV的分子表达谱和功能分析 [打印本页]
作者: admin 时间: 2019-6-20 09:29
标题: Cell Reports: 肿瘤相关巨噬细胞EV的分子表达谱和功能分析
Cell Reports: 肿瘤相关巨噬细胞来源EV的分子表达谱和功能分析显示出抗肿瘤免疫作用
包括外泌体在内的细胞外囊泡(EV)调节了肿瘤生物学的多个方面。肿瘤相关巨噬细胞(TAM)分泌EV,但其分子特征和功能在肿瘤组织微环境中尚有待研究。在这项研究里,来自瑞士洛桑联邦理工学院的研究人员分析了肿瘤相关巨噬细胞衍生EV的蛋白质组学和脂质组学特征,发现肿瘤相关巨噬细胞来源的EV 可能具有抗肿瘤免疫作用,表现出与其来源细胞不同的生物学效应。
细胞外囊泡(EV)是由几乎所有细胞类型释放的异质性的膜囊泡。EV可以根据其大小和亚细胞来源进行分类:外泌体(30-150 nm)来自晚期多泡体,而微泡(100-1000 nm)和凋亡小体(100-5,000 nm)分别来自正常稳态条件下和细胞死亡期间质膜的脱落。EV介导的细胞间通讯研究已成为肿瘤生物学研究的热点。肿瘤来源的EV与肿瘤进展期间的各种生物学过程有关,包括肿瘤免疫、血管生成、肿瘤转移和肿瘤治疗抗性等。
目前,大多数研究集中于从体外培养的肿瘤细胞中分离的EV,然后进行表征。一些研究也检测了组织衍生EV的性质,其中包括直接从肿瘤中分离EV进行检测。然而,肿瘤组织中的细胞类型复杂,不仅仅肿瘤细胞可以产生EV,组织中其他各类肿瘤微环境(TME)细胞均会产生EV,这些EV的起源、性质和对肿瘤微环境和远处器官的影响仍然在很大程度上还是未知的。
在肿瘤组织中,肿瘤细胞与宿主的许多其他类型细胞混合,共同调节肿瘤进展和对治疗的反应性。在免疫细胞中,肿瘤相关巨噬细胞(TAM)是实体肿瘤中的微环境成分,调节肿瘤进展的若干方面,包括血管生成、免疫抑制和肿瘤细胞侵袭和转移。巨噬细胞的遗传性减低可以通过干扰血管生成和转移来减缓肿瘤进展。集落刺激因子1受体(CSF1R)对TAM的发展和存活至关重要。抗CSF1R的单克隆抗体2G2可以有效地消耗TAM,并且与一些抗血管生成药物、免疫抑制剂和共刺激分子激动剂共同组合提高肿瘤治疗效果。在小鼠中的的临床前研究中,消耗巨噬细胞或重编程巨噬细胞同时与一些一线抗肿瘤疗法相结合,已经在实验和进行当中。
肿瘤相关巨噬细胞调节着肿瘤微环境中各种宿主细胞类型的功能,包括血管细胞和淋巴细胞,这些调节主要涉及细胞因子和基质重塑酶类的产生。巨噬细胞来源的EV对肿瘤组织中这些微环境细胞的影响以及潜在功能研究很少。肿瘤相关巨噬细胞的表型丰富并且功能可塑,这取决于它们所在肿瘤微环境的确切性质。目前,大多数研究集中于从培养的巨噬细胞中纯化EV,而从肿瘤组织中分离巨噬细胞衍生的EV在技术上没有公认的研究方法。
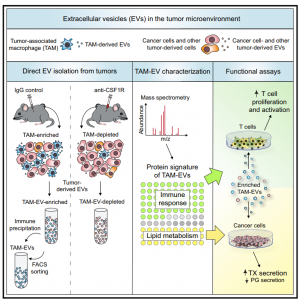
在这项研究中,研究人员描述了肿瘤相关巨噬细胞衍生EV的蛋白质组学和脂质组学特征,以及这些EV对肿瘤细胞和T细胞的影响。研究人员从小鼠中富集TAM释放的EV(TAM-EV),并进行定量以及蛋白质组学、脂质组学分析。与其来源TAM相比,TAM-EV呈现与Th1 / M1极化特征相关的分子表达谱、炎症和免疫应答增强、以及更好的患者预后。因此,富集的TAM-EV能够促进T细胞增殖和离体活化。TAM-EV还含有生物活性脂质和生物合成酶,其可以改变肿瘤细胞中的促炎症信号传导。因此,尽管TAM主要作用是免疫抑制,但TAM分泌的EV可能具有激活抗肿瘤免疫的作用。
参考文献:Cianciaruso C, Beltraminelli T, Duval F, Nassiri S, Hamelin R, Mozes A, Gallart-Ayala H, Ceada Torres G, Torchia B, Ries CH, Ivanisevic J, De Palma M. Molecular Profiling and Functional Analysis of Macrophage-Derived Tumor Extracellular Vesicles. Cell Rep. 2019 Jun 4;27(10):3062-3080.e11.
附件已隐藏,回复该贴可查看附件
作者: muzi1987xiaohao 时间: 2019-6-21 08:47
感谢分享
作者: ffzhao 时间: 2019-6-21 12:12
66666666666666666666666666666
作者: hermmoon 时间: 2019-6-21 13:22
谢谢分享
作者: Taichi 时间: 2019-6-21 15:17
感谢分享
作者: 墨清 时间: 2019-6-24 11:59
感谢分享
作者: 奥比克 时间: 2019-6-24 20:47
赞赞赞赞赞赞赞赞
作者: suchaoyue 时间: 2019-7-1 14:50
6666666666666
作者: 吴绍聪 时间: 2019-8-13 13:06
6666666666666666666
| 欢迎光临 外泌体之家 | 细胞外膜泡领域核心平台—exosomes & microvesicles—小膜泡大作用 (http://exosome.com.cn/) |
Powered by Discuz! X3.3 |