Molecular Therapy: 工程化细胞外小囊泡sEVsRVG 通过递送抗病毒siRNA靶向胎鼠头部抑制ZIKV感染并减轻病毒造成的鼠小头症
寨卡病毒(ZIKV)是黄病毒科黄病毒属的单股正链RNA病毒。2015-2017年,ZIKV在南美、东南亚等地区爆发,造成数百万人感染,尤其是ZIKV感染导致的新生儿小头畸形和格林-巴利综合征1,给公共健康带来了巨大的挑战。目前针对ZIKV感染尚无批准使用的预防疫苗和治疗药物。2021年11月10日,南京大学吴稚伟团队在Molecular Therapy上发表了题为 “sEVsRVG selectively deliversantiviral siRNA to fetus brain, inhibits ZIKVinfection and mitigates ZIKV induced microcephaly in mouse model”的研究论文。该论文揭示了工程化细胞外小囊泡sEVsRVG良好的靶向穿透力及其对孕期病毒感染造成的胎鼠脑部损伤中的治疗作用。南京大学博士生张瑞为该论文第一作者,吴稚伟教授和医学院苏北人民医院王永祥教授为该论文共同通讯作者。这项工作得到了“十三五传染病重大专项”及国家自然科学基金的支持。
图1:研究工作示意图
ZIKV经蚊虫叮咬感染孕妇可由母亲通过垂直传播传染给胎儿,诱发新生儿的小头症。因为胎盘的特殊致密结构使得许多治疗药物难以到达胎儿,这为开发治疗ZIKV感染的药物带来挑战性。在早期的研究中发现,细胞外小囊泡表现出卓越的穿越胎盘和到达胎儿体内的能力,可以携带核酸、蛋白质或其他小分子作为治疗药物递送到特定位置。
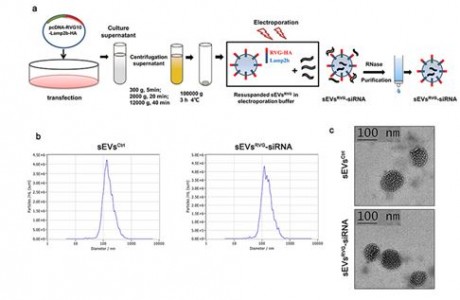
图2:sEVsRVG-siRNA的制备和表征
为了开发一种能够穿越胎盘和血脑屏障的特异性抗病毒疗法来治疗ZIKV引起的小头症,研究者设计了靶向脑部神经的细胞外小囊泡(sEVs[size=0.625em]RVG)并装载抗病毒siRNA(ZIKV特异性siRNA)来抑制ZIKV。细胞外小囊泡(sEVs[size=0.625em]RVG)的脑部神经特异性靶向是通过将sEVs膜蛋白lamp2b和神经靶向性的狂犬病毒糖蛋白衍生肽(RVG)融合递呈在细胞外囊泡上,在细胞及动物水平验证了sEVs[size=0.625em]RVG-siRNA的抗病毒能力。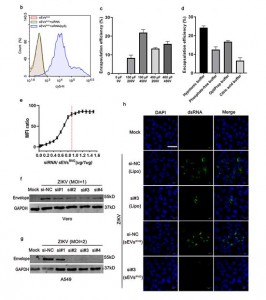 图3:sEVsRVG-siRNA装载siRNA条件的优化及其在细胞水平上的抗病毒能力 图3:sEVsRVG-siRNA装载siRNA条件的优化及其在细胞水平上的抗病毒能力
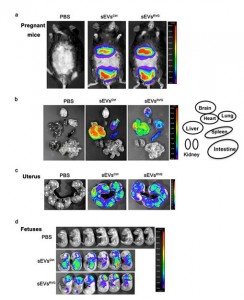 图4:孕鼠模型证明sEVsRVG可跨越胎盘屏障到达靶向组织 图4:孕鼠模型证明sEVsRVG可跨越胎盘屏障到达靶向组织
通过尾静脉给孕鼠注射sEVs[size=0.625em]RVG发现其能够穿透胎盘屏障及血脑屏障到达胎鼠脑部神经细胞,验证了sEVs[size=0.625em]RVG良好的组织穿透力及神经靶向性。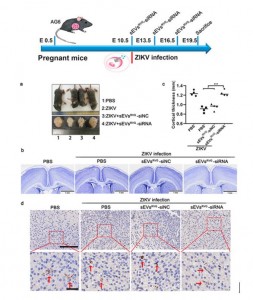 图5:sEVsRVG-siRNA保护胎鼠免受ZIKV感染并缓解ZIKV引起神经炎症和神经系统损伤 图5:sEVsRVG-siRNA保护胎鼠免受ZIKV感染并缓解ZIKV引起神经炎症和神经系统损伤
最后,研究人员通过用ZIKV感染怀孕AG6小鼠构建了胎鼠小头症模型,并在孕鼠攻毒0/3/6天后给予sEVs[size=0.625em]RVG-siRNA进行治疗,sEVs[size=0.625em]RVG-siRNA治疗组相对于其他组在孕鼠胎盘、子宫及胎鼠脑部有较为明显的抑制病毒作用;饲养胎鼠到一定天数后,对比发现治疗组胎鼠的小头畸形有明显缓解并且sEVs[size=0.625em]RVG-siRNA的治疗降低了病毒造成的神经损伤及炎症。在未来,针对孕期病毒感染造成的胎儿脑部损伤,RVG修饰细胞外小囊泡装载抗病毒小分子靶向治疗或许是种潜在可能。该研究工作也引起了国外相关媒体的关注。
参考文献:sEVs RVG selectively delivers antiviral siRNA to fetus brain,inhibits ZIKV infection and mitigates ZIKV-induced microcephaly in mouse model.MolTher, 2021,2;S1525-0016(21)00516-5.
|  /1
/1 
 |Archiver|手机版|外泌体之家 | exosomes & microvesicles
|Archiver|手机版|外泌体之家 | exosomes & microvesicles
